Teriflunomid – Čo nám hovorí nová analýza
o jeho účinnosti vzhľadom na vek
Odborná redakcia SM News
Skleróza multiplex (SM) predstavuje chronické zápalové demyelinizačné a neurodegeneratívne ochorenie centrálneho nervového systému. Prvé klinické príznaky sa zvyčajne manifestujú medzi 20. – 40. rokom života. Epidemiologické štúdie poukazujú na nárast priemerného veku pacientov s SM. Napríklad v USA je približne 14 % pacientov s SM vo veku ³ 65 rokov. Zvýšenie prevalencie bez ohľadu na vek dokazujú údaje napríklad z Kanady, Nórska, Nového Zélandu a USA. Dlhodobé registre pacientov so SM z Austrálie, Kanady a Talianska taktiež potvrdzujú zvýšenie prevalencie SM vo vyšších vekových skupinách. Možným vysvetlením je všeobecné starnutie populácie a pokrok medicíny v liečbe SM, s čím súvisí dožívanie sa vyššieho veku pacientov postihnutých SM. Vedie sa diskusia, či spolu s prevalenciou vo vyššom veku nerastie aj incidencia. Výsledky sú v tomto smere nejednoznačné. Niektorí autori dávajú uvedenú skutočnosť do súvislosti so zlepšenou diagnostikou ochorenia vrátane širšieho využitia moderných diagnostických metód, akými sú napr. zobrazovacie metódy (Dobson & Giovannoni, 2019; Vaughn et al., 2019).

S rastúcou prevalenciou SM vo vyšších vekových skupinách zákonite vzniká otázka ohľadne účinnosti a bezpečnosti liekov používaných v liečbe SM. Randomizované klinické štúdie zvyčajne nedostatočne pokrývajú skupinu starších pacientov (Vaughn et al., 2019).
Podľa niektorých metaanalýz môžu mať lieky modifikujúce ochorenie, resp. imunomodulačná ochorenie modifikujúca liečba (podľa zvolenej definície autorov) účinnosť ovplyvnenú vekom pacienta v prípade relaps-remitujúcej formy M alebo progresívnej SM. S rastúcim vekom pacienta môže účinnosť liekov používaných v liečbe SM klesať. Uvažuje sa
o rôznych príčinách: trvanie samotného ochorenia, vplyv užívaných liekov na SM
v minulosti, zmeny
v imunitnom systéme
v súvislosti
s vekom a/alebo samotným ochorením (Signori et al., 2015; Weideman et al., 2019).
Nedávno publikovaná post hoc analýza pacientov so SM liečených teriflunomidom v dávke 14 mg/deň bola zameraná na hodnotenie účinnosti a bezpečnosti lieku vzhľadom na vek. Analyzovali sa štúdie z fázy II.
a III. klinického skúšania
TEMSO,
TOWER,
TENERE,
TOPIC (spolu 1 978 pacientov)
a štúdie z reálnej klinickej praxe
Teri-PRO (928 pacientov)
a TAURUS-MS I (1 126 pacientov). Klinické štúdie
TEMSO,
TOWER,
TENERE,
TOPIC vrátane rozšírenia trvali vyše 13 rokov, štúdie vychádzajúce z reálnej klinickej praxe
Teri-PRO 48 týždňov
a TAURUS-MS I vyše 2 roky. Do štúdie
TAURUS-MS I boli zaradení pacienti
s relaps-remitujúcou formou SM, do štúdií
TEMSO,
TOWER,
TENERE,
Teri-PRO pacienti
s relapsujúcou SM
a do štúdie
TOPIC pacienti
s klinicky izolovaným syndrómom (McDonald kritériá z roku 2005). V klinických štúdiách sa hodnotenie pacientov uskutočnilo podľa metódy
Intent to Treat. Detaily
k uvedeným štúdiám je možné nájsť
v literatúre. Pacienti zaradení do uvedených štúdií boli stratifikovaní podľa veku
v čase zaradenia do štúdie: ⩽ 25, > 25 a ⩽ 35, > 35 a ⩽ 45
a > 45 rokov. V štúdiách
Teri-PRO a TAURUS-MS I pribudla ešte veková skupina > 55 rokov (Oh et al., 2021).
Aj keď randomizované kontrolované štúdie predstavujú zlatý štandard
v hodnotení liekov,
veľkým prínosom je zaradenie dvoch štúdií z reálnej klinickej praxe vzhľadom na známu skutočnosť, že dizajn klinických štúdií sa môže v rôznej miere líšiť od reálnej klinickej praxe. Jednou zo základných otázok je hodnotenie účinnosti
a bezpečnosti lieku
v skupine pacientov, ktorí neboli zahrnutí do randomizovaných štúdií alebo nepredstavovali dostatočne veľkú skupinu
v rámci štúdií,
a to bývajú veľmi často seniori. V súčasnosti rastie požiadavka aj na výsledky z reálnej klinickej praxe z hľadiska komplexného hodnotenia lieku (Trojano et al., 2017).
Podľa autorov analýzy bola neadjustovaná ročná miera relapsov (angl. Annualized Relapse Rate (ARR)) pre štúdie z fázy II. a III. klinického skúšania nízka a pohybovala sa v intervale 0,18 – 0,30 a v štúdiách z reálnej klinickej praxe Teri-PRO 0,10 – 0,35 a TAURUS-MS I 0,14 – 0,35 v definovaných vekových skupinách (Oh et al., 2021).
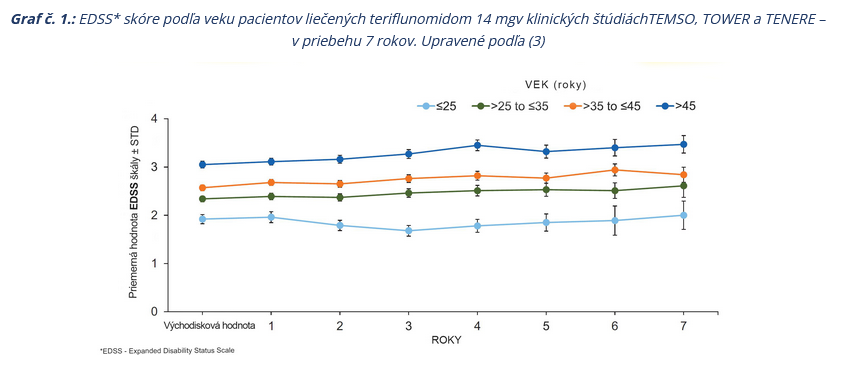
Pri vstupe pacientov do štúdie hodnoty EDSS škály (angl. Expanded Disability Status Scale (EDSS)) rástli
s vekom, ale vykazovali stabilitu počas trvania štúdie.
Priemerný nárast hodnôt EDSS škály za 7 rokov oproti východiskovej hodnote v štúdiách TEMSO, TOWER, TENERE, TOPIC podľa vekových skupín predstavoval: ⩽ 25 rokov + 0,59; > 25 a ⩽ 35 rokov + 0,46; > 35 a ⩽ 45 rokov + 0,35 a > 45 rokov + 0,81. Obdobné hodnoty boli zaznamenané v štúdii Teri-PRO po 48 týždňoch: ⩽ 25 rokov – 0,18; > 25 a ⩽ 35 rokov + 0,03; > 35 a ⩽ 45 rokov + 0,05, > 45 a ⩽ 55 rokov + 0,13 a > 55 rokov – 0,05 a TAURUS-MS I po 2 rokoch: ⩽ 25 rokov – 0,07; > 25 a ⩽ 35 rokov – 0,07; > 35 a ⩽ 45 rokov + 0,14, > 45 a ⩽ 55 rokov +0,08 a > 55 rokov + 0,33 (Oh et al., 2021).
Výskyt nežiaducich účinkov sa
v štúdiách z fázy II
a III klinického skúšania vyskytoval
v intervale 78,4 – 90,7 % vo všetkých vekových skupinách
v sledovanom období vyše 13 rokov. V štúdiách, ktoré vychádzali z podmienok reálnej klinickej praxe, to bolo
v štúdii
Teri-PRO 78,4 – 85,0 %
v období 48 týždňov
a v štúdii
TAURUS-MS I 29,2 – 37,7 % za obdobie 2 rokov (Oh et al., 2021).
Autori analýzy zhrnuli výsledky takto (Oh et al., 2021):
- teriflunomid preukázal svoju účinnosť bez ohľadu na vek zaradených pacientov do klinických štúdií,
- bezpečnosť lieku bola vo všeobecnosti konzistentná vo všetkých sledovaných vekových skupinách.
Výsledky analýzy sú v súlade aj s inými publikovanými hodnoteniami teriflunomidu. Klinické štúdie z fázy II. a III. (vrátane ich rozšírenia), klinické štúdie fázy IV. a údaje z reálnej praxe potvrdzujú jeho dlhodobú účinnosť, bezpečnosť a znášanlivosť. Teriflunomid má výrazný účinok na neurodegeneratívne procesy, čo sa prejavuje aj jeho vplyvom na zachovanie objemu mozgu a spomalenie progresu zdravotného postihnutia (Miller, 2021).
Literatúra
- Dobson, R., Giovannoni, G. (2019): Eur. J. Neurol., 26, 27–40
- Miller, A.R. (2021): Neurodegener. Dis. Manag., 11, 387–409
- Oh, J. et al. (2021): J. Cent. Nerv. Syst. Dis., 13, 1–11
- Signori, A. et al. (2015): Eur. J. Neurol., 22, 960–966
- Trojano, M. et al. (2017): Nature Rev. Neurol., 13, 105-118
- Vaughn, C.B. et al. (2019): Nature Rev. Neurol., 15, 329-342
- Weideman, A.M. et al. (2019): Front. Neurol., 8, 577

 Výskyt nežiaducich účinkov sa v štúdiách z fázy II a III klinického skúšania vyskytoval v intervale 78,4 – 90,7 % vo všetkých vekových skupinách v sledovanom období vyše 13 rokov. V štúdiách, ktoré vychádzali z podmienok reálnej klinickej praxe, to bolo v štúdii Teri-PRO 78,4 – 85,0 % v období 48 týždňov a v štúdii TAURUS-MS I 29,2 – 37,7 % za obdobie 2 rokov (Oh et al., 2021).
Autori analýzy zhrnuli výsledky takto (Oh et al., 2021):
Výskyt nežiaducich účinkov sa v štúdiách z fázy II a III klinického skúšania vyskytoval v intervale 78,4 – 90,7 % vo všetkých vekových skupinách v sledovanom období vyše 13 rokov. V štúdiách, ktoré vychádzali z podmienok reálnej klinickej praxe, to bolo v štúdii Teri-PRO 78,4 – 85,0 % v období 48 týždňov a v štúdii TAURUS-MS I 29,2 – 37,7 % za obdobie 2 rokov (Oh et al., 2021).
Autori analýzy zhrnuli výsledky takto (Oh et al., 2021):



